A Medicina é a Ciência de lidar com a incerteza. Só a questão, colocada repetida e sistematicamente, pode aligeirar o peso da dúvida e da consequência. É importante duvidar, mesmo do “óbvio”, questionar o “tradicional”. Por exemplo, o tratamento. O fármaco. As doses. O timing.
A pergunta de hoje é: porque é que o bolus intravenoso de corticóide (metilprednisolona) em dose alta é de 1 grama?
A resposta, quando se procura nas fontes primárias, é surpreendente. Revela porque é que todos os médicos e investigadores deveriam, têm, de ser historiadores. E diz muito sobre como surge, e como se transmite, o conhecimento médico.
Birmingham, 1951
Em Maio de 1951, Billingham, Krohn e Medawar publicaram no British Medical Journal um importante estudo sobre transplantação (Billingham et al., 1951). O objectivo era perceber se os corticóides prolongavam a sobrevivência de enxertos de pele entre coelhos geneticamente distintos (portanto com sistemas imunitários que “desconfiariam” de um órgão, mesmo a pele, que não fosse “deles”). A dose escolhida foi de 10 mg por dia de acetato de cortisona, apenas recentemente descoberta.
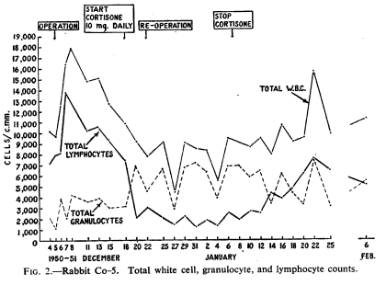
A experiência funcionou, quadruplicando a sobrevivência do enxerto. Os autores hipotizaram que o mecanismo era a supressão da resposta imunológica do receptor do transplante, documentada por uma linfopenia (redução dos linfócitos) persistente ao longo do tratamento. Quanto mais linfócitos eram destruídos, e por mais tempo, melhor a sobrevivência do enxerto.
Peter Medawar viria a receber o Prémio Nobel da Fisiologia ou Medicina em 1960, precisamente pelos seus contributos para a área da transplantação. O que ninguém poderia prever em 1951 é que aqueles 10 mg de cortisona em coelhos de laboratório iriam determinar, décadas depois, o protocolo de tratamento de doenças autoimunes humanas.
Denver, 1970 e Glasgow, 1971
A transplantação humana só se viria a estabelecer em torno a 1965, quinze anos após o estudo de Billingham e Medawar, com a introdução de imunossupressão baseada em prednisolona e azatioprina. Estes regimes não eram tão eficazes como seria desejável. Quando surgia uma rejeição, a única opção era aumentar ainda mais as doses de corticóide oral.
É neste contexto de batalha contra a rejeição aguda que, em 1970, Coburg, Gray, Katz, Penn, Halgrimson e Starzl, da Universidade do Colorado, publicaram uma investigação sobre injecções intravenosas intermitentes de prednisolona em transplantados renais e em voluntários saudáveis (Coburg et al., 1970).
A tradução da dose animal para a dose humana está formulada no artigo de forma directa: “a dose intravenosa de 10 mg/kg de metilprednisolona no coelho era comparável a um total de 1 g de prednisolona no ser humano.” Mesmo usando a recém desenvolvida metilprednisolona (1957), mais potente e com menos efeitos laterais, era ainda a mesma dose de Medawar, convertida por equiparação de peso. Os autores mostraram que este 1 g produzia, no humano, uma linfopenia profunda com nadir às quatro horas, que persistia durante a maior parte do primeiro dia, com meia-vida plasmática de apenas 60 a 90 minutos.
O objectivo era exactamente o mesmo de 1951: a destruição máxima de linfócitos, pelo maior tempo possível, para suprimir a rejeição do enxerto, agora em humanos. Os próprios autores reconheciam que a prática havia “desenvolvido de forma mais ou menos empírica no tratamento de receptores de homoenxertos.”
O grama não resultou de um ensaio de dose-resposta.
Do outro lado do Atlântico, Bell e colaboradores, da Universidade de Glasgow, publicaram no Lancet os resultados de 1 g de prednisolona IV na reversão de episódios de rejeição aguda em 16 transplantados renais (Bell et al., 1971). Citavam Coburg et al. para justificar a escolha da dose: meia-vida curta, poucos efeitos laterais crónicos, capacidade linfocitolítica como mecanismo de acção. Obtiveram reversão em 86% dos episódios. A dose de 1 g ficava assim documentada em dois artigos favoráveis.
Nenhum testava a dose fora do contexto de transplante.
1976: a fronteira da autoimunidade é atravessada
Em Fevereiro de 1976, Cole e colaboradores, de St. Louis, publicaram no Journal of Pediatrics um estudo com oito crianças com glomerulonefrite (inflamação dos rins) grave (Cole et al., 1976). A dose foi de 30 mg/kg de metilprednisolona IV em seis dias alternados. Trinta mg/kg era a dose ponderada utilizada nos modelos animais por Coburg et al., agora aplicada a crianças segundo a prática pediátrica habitual de dosagem por peso corporal. Cole et al. citavam Bell et al. como justificação. A lógica era simples: se funcionava nos transplantes renais, a fisiopatologia era suficientemente semelhante para justificar a tentativa.
No mesmo ano, Cathcart e colaboradores publicavam no Lancet os resultados em sete doentes com glomerulonefrite lúpica (Cathcart et al., 1976). A dose foi de 1 g por dia durante três dias. Os autores descreveram que ficaram “inicialmente impressionados pelas semelhanças histológicas entre a biópsia renal de um desses doentes e a rejeição aguda de transplante renal.” A dose foi herdada directamente do contexto transplante, sem reavaliação para o novo contexto clínico.
Dois grupos, de forma independente, adoptavam, no mesmo ano, a dose do transplante para doenças autoimunes, por analogia e sem ensaio comparativo.
Portsmouth, 1977
Neild e Lee publicaram em 1977 dois casos de poliarteriite nodosa tratados com 30 mg/kg de metilprednisolona IV (Neild e Lee, 1977). A justificação estava formulada de forma explícita na introdução: ficaram “impressionados pela falta de toxicidade de doses altas de metilprednisolona IV no trabalho de transplantação renal.” Citavam Bell et al. e Feduska et al. como prova de eficácia. Reconheciam que “o uso de esteróides na poliarteriite nodosa e noutras doenças do colagénio é empírico.”
A vasculite tinha agora o mesmo protocolo. Também por herança.
A cadeia completa
Encontra-se assim o fio à meada, referência a referência:
Medawar 1951 (10 mg/dia de cortisona SC no coelho, linfopenia como objectivo) → Coburg 1970 (conversão para 1 g IV no humano, reconhecidamente empírica) → Bell 1971 (1 g IV em rejeição de transplante, eficácia estabelecida) → Cole 1976 (30 mg/kg em glomerulonefrite pediátrica, citando Bell) / Cathcart 1976 (1 g em lúpus, por analogia com transplante) → Neild 1977 (30 mg/kg em vasculite, citando transplante).
O objectivo para o qual esta dose foi originalmente concebida era maximizar e prolongar a destruição de linfócitos T para travar a rejeição de um órgão estranho. Nas doenças autoimunes, o objectivo é diferente: suprimir uma resposta inflamatória patológica, que pode ou não ser mediada celularmente, preservando tanto quanto possível as defesas contra infecção. Esta distinção nunca foi o ponto de partida de nenhuma validação prospectiva da dose.
O que a evidência tem mostrado
Já em 1976, e no mesmo domínio da transplantação, Alarcon-Zurita e Ladefoged, em Copenhaga, publicavam a sua experiência com doses altas de corticóide em 64 episódios de rejeição aguda em transplantados renais (Alarcon-Zurita e Ladefoged, 1976). Os resultados eram menos favoráveis do que os de Bell: reversão em apenas 60% dos episódios, com mortalidade de 44% ao ano. Mais importante, os autores observaram que doses totais de metilprednisolona superiores a 3 a 5 g não melhoravam as taxas de reversão mas aumentavam as complicações. Os doentes que receberam doses de 0,5 g por dia tinham resultados comparáveis aos que receberam 1 g. A sugestão de que menos poderia ser suficiente estava ali, em 1976, no mesmo ano em que o 1 g se instalava como padrão.
Outros estudos comparativos chegaram tarde e em pequeno número. Um ensaio duplamente cego de 1987 comparou 100 mg com 1000 mg de metilprednisolona em lúpus grave. Não encontrou diferença clínica significativa (Edwards et al., 1987). Uma análise retrospectiva de 2002 mostrou que 500 mg eram tão eficazes quanto 1 g, com menos infecções (Badsha et al., 2002). O risco infeccioso é proporcional à dose e concentra-se sobretudo no primeiro ano após a exposição (Barbulescu et al., 2023). A resposta às vacinas fica comprometida com doses elevadas (Figueras Nart et al., 2025), o que cria um ciclo difícil de quebrar precisamente nos doentes que mais necessitam de protecção.
Há uma razão farmacológica para estas observações. A classificação de Buttgereit estabelece que os receptores intracelulares de glucocorticóides ficam praticamente saturados a doses muito inferiores a 500 mg (Buttgereit et al., 2004). Acima desse limiar, os mecanismos genómicos clássicos, que mediam a maior parte dos efeitos anti-inflamatórios, não aumentam com a dose. O que 1 g acrescenta são sobretudo efeitos físico-químicos em membranas celulares, dependentes de concentrações muito elevadas, e uma inibição mais profunda da desgranulação neutrofílica. Doses de 100 a 250 mg IV provavelmente já esgotam todos os mecanismos relevantes para a supressão da inflamação autoimune.
Em 2006 (há vinte anos!), Franchin e Diamond formularam a questão de forma directa: há evidência de eficácia equivalente com doses mais baixas, mas nenhum estudo conclusivo havia sido desenhado para responder à pergunta (Franchin e Diamond, 2006).
As normas orientadoras internacionais mais recentes da EULAR para o lúpus, a nefrite lúpica e a vasculite associada a ANCA reflectem o reconhecimento crescente deste problema: os intervalos de dose recomendados para o bolus IV tornaram-se mais explícitos no limite inferior, as doses orais subsequentes foram reduzidas, e a retirada progressiva dos corticóides passou a ser um objectivo declarado (Fanouriakis et al., 2024; Hellmich et al., 2023; Tamirou et al., 2025). O intervalo do bolus continua largo, de 250 a 1000 mg, mas o chão está a descer. A evidência aponta para baixo. A tradição aponta para 1 g.
Uma reflexão final
Medawar fazia ciência fundamental de primeira ordem. Coburg e Starzl tentavam salvar enxertos em doentes que morriam de rejeição. Bell obteve resultados clínicos impressionantes. Cole, Cathcart e Neild extrapolaram com a melhor evidência de que dispunham, perante doentes em situação grave.
A medicina avança por acumulação de conhecimento, e parte desse conhecimento chega-nos por herança, por tradição, por transmissão oral entre gerações de médicos. Nem tudo o que é transmitido foi validado no contexto em que o usamos. Nem tudo o que parece óbvio foi alguma vez questionado com rigor.
É precisamente aí que reside a função do clínico-investigador: não apenas aplicar o conhecimento existente, mas questionar a sua origem, testar os seus fundamentos, e perceber quando uma resposta que sempre pareceu óbvia ainda está à espera da pergunta certa. A tradição não é prova. A ausência de questionamento não é consenso. E a repetição de uma prática ao longo de décadas não a torna na mais correcta.
A dose de 1 g de metilprednisolona que um doente com doença imunomediada emergente recebe em 2026 tem a sua origem em trabalhos de Peter Medawar, em coelhos, para um problema completamente diferente. Chegou até nós por uma cadeia de analogias razoáveis, cada uma delas com resultados suficientemente bons, numa época em que a alternativa era a morte certa. Estabeleceu-se como status quo, ao ponto de ninguém ter ainda estudado, cabalmente, se será possível fazer o mesmo com menos.
Em 1976, Alarcon-Zurita e Ladefoged já sugeriam 0,5 g como alternativa eficaz (Alarcon-Zurita e Ladefoged, 1976). A evidência que se tem vindo a acumular desde então valida-os. Está na hora de começarmos a mudar a tradição.
Referências
Alarcon-Zurita A, Ladefoged J. Treatment of acute allograft rejection with high doses of corticosteroids. Kidney Int. 1976;9:351–354.
Badsha H, Kong KO, Lian TY, et al. Low-dose pulse methylprednisolone for systemic lupus erythematosus flares is efficacious and has a decreased risk of infectious complications. Lupus. 2002;11(8):508–513.
Barbulescu A, et al. Glucocorticoid exposure and the risk of serious infections in rheumatoid arthritis: a marginal structural model application. Rheumatology. 2023;62(10):3391–3399.
Bell PRF, Calman KC, Wood RFM, et al. Reversal of acute clinical and experimental organ rejection using large doses of intravenous prednisolone. Lancet. 1971;1:876–880.
Billingham RE, Krohn PL, Medawar PB. Effect of cortisone on survival of skin homografts in rabbits. Br Med J. 1951;1(4716):1157–1163.
Buttgereit F, Straub RH, Wehling M, Burmester GR. Glucocorticoids in the treatment of rheumatic diseases: an update on the mechanisms of action. Arthritis Rheum. 2004;50(11):3408–3417.
Cathcart ES, Idelson BA, Scheinberg MA, Couser WG. Beneficial effects of methylprednisolone “pulse” therapy in diffuse proliferative lupus nephritis. Lancet. 1976;1(7952):163–166.
Coburg AJ, Gray SH, Katz FH, Penn I, Halgrimson C, Starzl TE. Disappearance rates and immunosuppression of intermittent intravenously administered prednisolone in rabbits and human beings. Surg Gynecol Obstet. 1970;131(5):933–942.
Cole BR, Brocklebank JT, Kienstra RA, Kissane JM, Robson AM. “Pulse” methylprednisolone therapy in the treatment of severe glomerulonephritis. J Pediatr. 1976;88(2):307–314.
Edwards JC, Snaith ML, Isenberg DA. A double blind controlled trial of methylprednisolone infusions in systemic lupus erythematosus using individualised outcome assessment. Ann Rheum Dis. 1987;46(10):773–776.
Fanouriakis A, et al. EULAR recommendations for the management of systemic lupus erythematosus: 2023 update. Ann Rheum Dis. 2024;83(1):15–29.
Figueras Nart I, et al. Glucocorticoid dosing and implications for vaccination: evolution of global definitions. Clin Infect Dis. 2025. https://doi.org/10.1093/cid/ciae578
Franchin G, Diamond B. Pulse steroids: How much is enough? Autoimmunity Reviews. 2006;5(2):111–113.
Hellmich B, et al. EULAR recommendations for the management of ANCA-associated vasculitis: 2022 update. Ann Rheum Dis. 2023. https://doi.org/10.1136/ard-2022-223764
Neild GH, Lee HA. Methylprednisolone pulse therapy in the treatment of polyarteritis nodosa. Postgrad Med J. 1977;53(621):382–387.
Tamirou F, et al. EULAR recommendations for SLE with kidney involvement: 2025 update. Ann Rheum Dis. 2025. https://doi.org/10.1016/S0003-4967(25)04412-7

Deixe um comentário